Yksinkertainen höyryn puristusjakso
Pari puristussykli käytetään jäähdytykseen kaasusyklien sijaan; piilevän lämmön käyttäminen mahdollistaa paljon suuremman määrän lämpöä talteenotettavan kylmäainevirtauksen. Tämä tekee laitteet mahdollisimman kompakti.
Neste kiehuu ja haihtuu - vaihda neste- ja kaasumaisen tilan välillä lämpötilassa, joka riippuu sen jäätymispisteessä olevasta paineesta ja kriittisestä lämpötilasta (katso kuva 2.2). Keittäessään hänen tulisi saada piilevä haihtumislämpö ja piilevän lämmön tiivistyminen siirtyy.
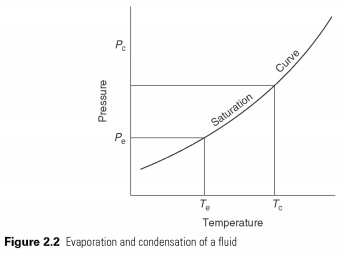
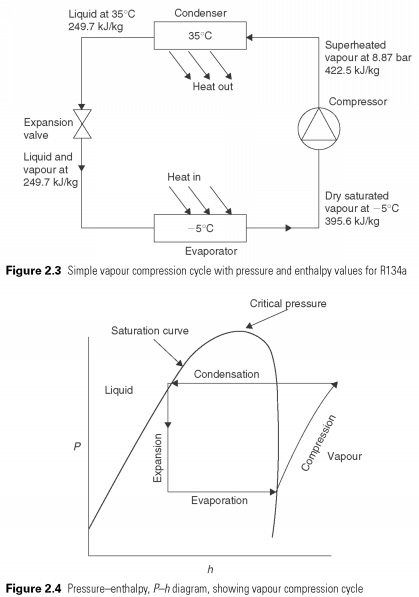
Lämpö on nestemäisessä tilassa alhaisissa lämpötiloissa ja paineissa, mikä tuottaa piilevän lämmön, jotta se haihtuisi. Sitten pari puristetaan automaattisesti korkeaan paineeseen, sen piilevää lämpöä vastaava kyllästymislämpötila voidaan kieltäytyä, joten hän muuttuu takaisin nesteeksi. Jakso on esitetty kuvassa 2.3. Lämpökantajan jäähtymisen vaikutus haihtumisprosessissa, joka on muutos entalpiassa nesteen ja höyryn välillä, jättäen РёСЃРїР ° СЂРёС,РμР »СЊ.
Jotta tätä prosessia voitaisiin tutkia tarkemmin, jäähdytysinsinöörit käyttävät paine-entalpiaa tai Ph-taulukkoa (kuva.
2.4). Tämä kaavio on kätevä tapa kuvata aineen neste- ja kaasufaaseja. Pystysuoralla akselilla paine P ja vaakatasossa h, entalpia. Kylläisyyskäyrä määrittelee puhtaan nestemäisen ja puhtaan kaasun tai höyryn rajan. Alue näytti höyryä, nestemäistä ylikuumennettua höyryä. Alue on merkitty nestemäisellä, jäähdytetyllä nesteellä. Yläkäyrän yläpuolella olevissa paineissa nesteellä ja höyryllä ei ole eroa. Tämän paineen yläpuolella kaasua ei voida nesteyttää. Tätä kutsutaan kriittiseksi paineeksi. Käyrän alla olevalla alueella, ts. Nesteen ja höyryn seos.
Yksinkertainen höyryn puristusjakso on päällä Ph-kaaviossa kuvassa 2.4. Jäähdytysnesteen haihtumis- tai haihdutusprosessi on vakiopaineprosessi ja siten se on vaakasuora viiva. Höyryn puristamiseen käytetyn energian puristusprosessissa muuttuu lämmöksi ja nostaa sen lämpötilaa ja entalpiaa, niin että höyryn puristustilan lopussa kuumennetussa kaaviossa ja kylläisyyskäyrän ulkopuolella. Prosessi, jossa puristuslämpö nostaa kaasun entalpiaa, jota kutsutaan adiabaattiseksi puristukseksi. Höyryt on jäähdytettävä ennen kuin kondensoituminen voi alkaa. Lopullinen puristuslämpötila on melkein aina alle tiivistyvä lämpötila kuten on esitetty, ja siksi tietty määrä lämpöä hylätään lämpötiloissa, jotka ovat kondensaation lämpötilan yläpuolella. Tämä edustaa poikkeamista ihanteellisesta jaksosta. Varsinainen kondensaatioprosessi esitetään vaakasuorista viivoista kylläisyyskäyrän sisällä.
Kun yksinkertainen höyryn puristusjakso näkyy lämpötila-entropiakaaviossa (kuva 2.5), poikkeamat taaksepäin käyvästä Carnot-syklisestä voidaan tunnistaa varjostettujen paikkojen perusteella. Adiabaattinen puristusprosessi jatkuu sen pisteen ulkopuolella, missä tiivistymislämpötila saavutetaan. Varjostettu kolmio edustaa ylimääräistä työmäärää, joka voidaan välttää, jos puristusprosessi muuttuu isotermiseksi (ts. Vakiolämpötilaan) sillä hetkellä, kun se jatkuu, kunnes lauhdepaine saavutetaan.
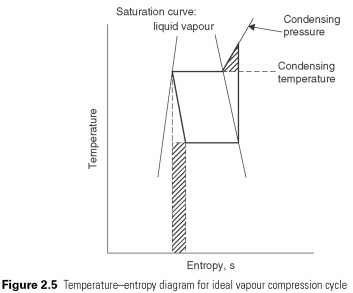
Prosessin jatkuvan entalpian laajeneminen. Se on valmisteltava pystysuoran viivan muodossa Ph-kaaviossa. Lämpöä ei imeytyä tai hylätä, kun neste laajenee vain venttiilin läpi. Paineen vähentämisen jälkeen venttiilissä pitäisi johtaa vastaavaan nestehöyryjen lämpötilan laskuun, jotta ne jäähtyvät. Nesteen tilavuus kasvattaa siten liittyvän kaasun venttiilimäärää, mikä johtaa sen nimeen paisuntaventtiili. Energiaa ei yritetä ottaa talteen esimerkiksi laajentumisprosessista. turbiinin avulla. Tämä on toinen poikkeama täydellisestä jaksosta. Työtä, joka voidaan mahdollisesti palauttaa, edustaa kuvan 2.5 varjostettu suorakulmio .....
|


