Bod varu
Teplota, při které kapalina vaří, není konstantní, ale mění se v závislosti na tlaku. Tudíž, zatímco se předpokládá, že teplota vroucí vody je 100C, platí to pouze při tlaku jedné standardní atmosféry (1.013 bar) a změně tlaku, odpařovací teplota, lze změnit (tabulka 1.1). Tuto vlastnost tlak-teplota lze znázornit graficky (viz obr. 1.4).
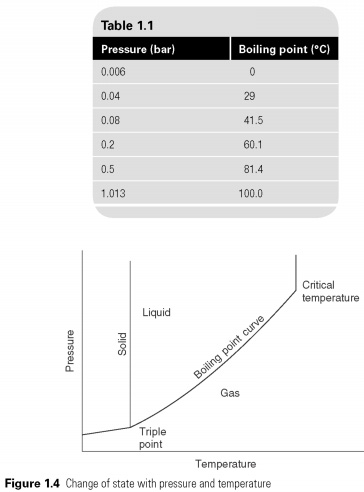
Bod varu látky je omezen na kritickou teplotu na horním konci, pro kterou nemůže existovat v kapalném stavu a na trojný bod ve spodní části, která zmrazení teplota. Mezi těmito dvěma limity, pokud kapalina pod tlakem nad tlakem vroucí, zůstane v kapalině, takže bude podchlazena pod nasycením, a pokud je teplota nad nasycením, bude to plyn a přehřáté. Pokud jsou v jednom případě kapalina i pára na dovolené a žádné jiné těkavé látky, musí podmínka ležet na hranici nasycení.
Tlak pod trojnásobným bodem tlaku, pevné tělo může přímo modifikovat plyn (sublimaci) a plyn se může měnit přímo na firmu, a to jak ve formaci РЊРІСѓРѕРєРёСЃСЊ uhlík sníh z uvolněného plynu.
Kapalná zóna nalevo od bodu varu linie k podchlazené kapalině.
V chladicím termínu „saturace“ se používá k popisu okraje kapalina / pára, nasycené páry se uvádějí ve formě čar a přehřáté pár pod řádkem.
....
|

