Ciclo simples de compressão de vapor
Par ciclo de compressão usado para resfriamento, de preferência aos ciclos de gás; o uso de calor latente permite recuperar muito mais fluxo de refrigerante. Isto faz equipamento o mais compacto possível.
Líquido para ferver e evaporar - alterne entre o estado líquido e gasoso a uma temperatura, que depende da pressão dentro do seu ponto de congelamento e da temperatura crítica (consulte a Fig. 2.2). Em ebulição, ele deve obter o calor latente da evaporação e a condensação no calor latente é transferida.
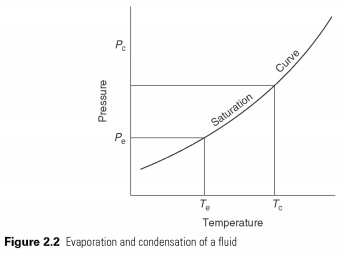
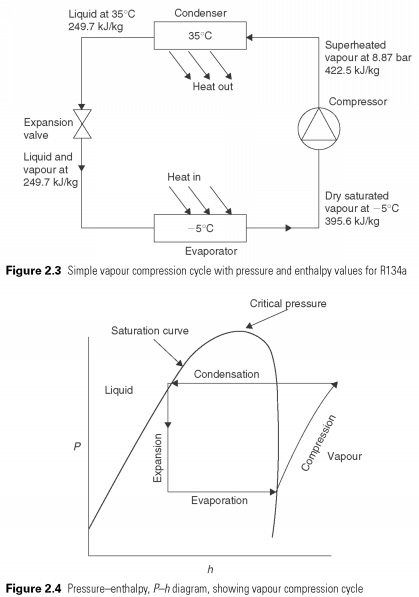
O calor está no estado líquido a baixas temperaturas e pressões, fornecendo o calor latente para evaporar. O par, então ele automaticamente é comprimido a alta pressão, a temperatura de saturação correspondente ao seu calor latente pode ser recusada, e ele volta a ser um líquido. O ciclo é mostrado na Fig. 2.3. O efeito do resfriamento do transportador de calor no processo de evaporação, que é a mudança na entalpia entre líquido e vapor, deixando РёСЃРїР ° ритель.
Para investigar esse processo mais de perto, os engenheiros de refrigeração usam entalpia de pressão ou gráfico de pH (Fig.
2.4). Este diagrama é uma maneira conveniente de descrever as fases líquida e gasosa da matéria. No eixo vertical, pressione P e horizontalmente, h, entalpia. A curva de saturação define os limites de um líquido puro e gás ou vapor puro. A região mostrou vapor, vapor superaquecido líquido. A região é marcada por líquido super-resfriado. A pressões acima da curva superior, não há distinção entre líquido e vapor. Acima dessa pressão, o gás não pode ser liquefeito. Isso é chamado de pressão crítica. Na área sob a curva, ou seja, uma mistura de líquido e vapor.
Ciclo simples de compressão de vapor está sobreposto ao gráfico de Ph na Fig. 2.4. O processo de evaporação ou evaporação do líquido de refrigeração é um processo de pressão constante e, portanto, é uma linha horizontal. No processo de compressão da energia utilizada para a compressão do vapor, transforma-se em calor e aumenta sua temperatura e entalpia, de modo que, no final do estado de compressão do vapor, nos gráficos superaquecidos e fora da curva de saturação. Um processo no qual o calor da compressão aumenta a entalpia do gás chamada compressão adiabática. Antes que a condensação possa começar, os vapores devem ser resfriados. A temperatura final de compressão está quase sempre abaixo temperatura de condensação como mostrado e, portanto, uma certa quantidade de calor é rejeitada em temperaturas acima da temperatura de condensação. Isso representa um desvio do ciclo ideal. O processo de condensação real é apresentado das linhas horizontais dentro da curva de saturação.
Quando simples ciclo de compressão de vapor é exibido no diagrama de temperatura-entropia (Fig. 2.5), os desvios do ciclo reverso de Carnot podem ser identificados pelos locais sombreados. O processo de compressão adiabática continua além do ponto em que a temperatura de condensação é atingida. O triângulo sombreado representa a quantidade adicional de trabalho que pode ser evitada se o processo de compressão mudar para isotérmico (ou seja, a temperatura constante) no momento em que continua até que a pressão de condensação seja atingida.
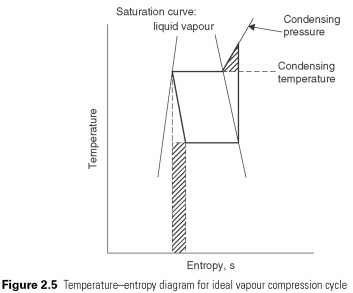
Expansão da entalpia constante do processo. Deve ser preparado na forma de uma linha vertical no esquema Ph. Nenhum calor é absorvido ou rejeitado durante a expansão do líquido apenas passa pela válvula. Depois de reduzir a pressão na válvula deve levar a um declínio correspondente na temperatura dos vapores líquidos piscando para remover a energia para o resfriamento. O volume de líquido aumenta, assim, a quantidade da válvula de gás associado, o que leva ao seu nome, o válvula de expansão. Nenhuma tentativa é feita para recuperar energia do processo de alargamento, por exemplo. com a ajuda da turbina. Este é o segundo desvio do ciclo perfeito. O trabalho que potencialmente poderia ser restaurado é representado pelo retângulo sombreado na Fig. 2.5 .....
|


